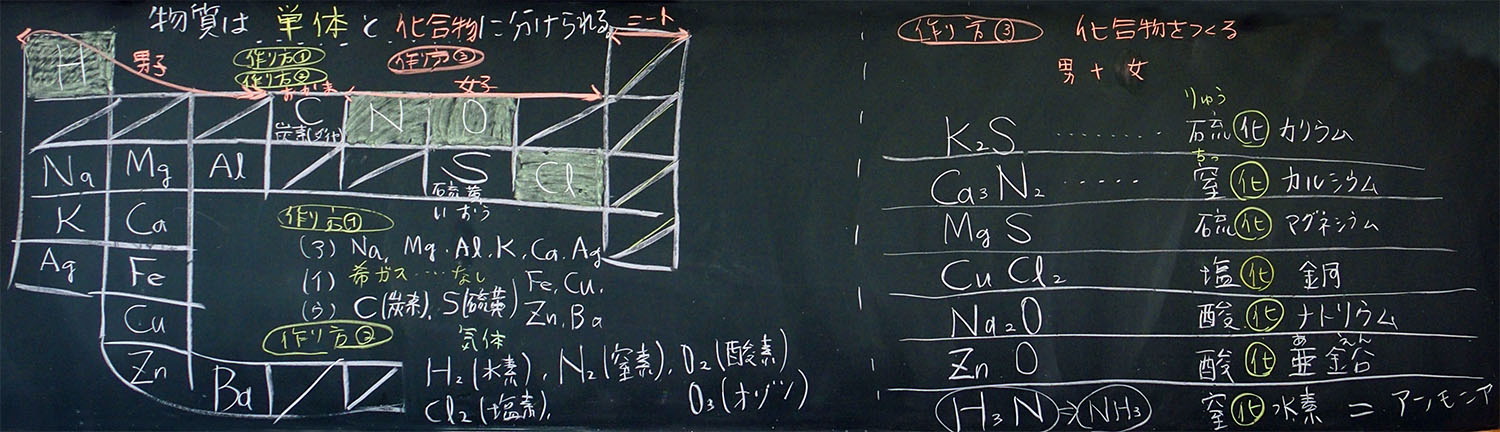第29時
実習4 いろいろな物質をつくろう2
2017 7 11(火)、12(水)
各教室
はじめに
ほとんど前の授業と同じ学習プリントを使って、同じような授業を行います。目的は化学の基礎となる粒、すなわち原子(元素)について深く理解することです。同じ内容を角度を変えてまとめたり、丁寧に復習したり、発展させたりします。どのように展開するかは、現場の子どもたちの様子から判断します。
|
準 備
| 生 徒 | 教 師 |
|
|
授業の流れ
前時と同じです。以下の囲み部分(黄色)は実習3『いろいろな物質を作ろう』の一部です。
休み時間のうちに教室へ入り、教卓に学習プリントをおきます。そして、「今日の学習プリントです。取りに来なさい」と指示します。さらに、「約束通り元素周期表の小テストを行います。始業のチャイムが鳴ってから2分後に開始します」と伝えます。 |
※前時との違いは2つです。
(1)覚えなければいけない16個以外は斜線で消してあること
(2)2学期の覚えることになる原子団4個の枠が追加してあること
追加された4つの枠については、今回書かなくてもよいことを指示してください。必ず質問されます。
(1)元素周期表の小テスト(10分) 「(時間になったら)時間です。始め!!」
|
5人ほど終了したタイミングで、自己採点の指示をします。正解は前の学習プリントにありますが、忘れた子どものために先生も板書してください。ポイントは、あっという間に正解を書きあげることです。子どもは先生がすらすら答える姿に憧れるものです。また、できない子どもの指導法についても再掲しますので参考にしてください。
|
(2)確認:周期表における位置について(2分)
「今日のテストは16個だけですが、最終的に16個だけでよいです(下図)。ただし、それでは面白くないという人は前の時間に紹介したように1番から20番まで覚えるとよいでしょう。宇宙をつくる元素について、一番軽い1番水素から20番までを知っていることは、まるで宇宙や自然のしくみを理解しているような気分にさせてくれます」
| 1 番 水素 |
2 番 | |||||||
| 3番 | 4番 | 5番 |
6 番 |
7 番 窒素 |
8 番 酸素 |
9番 | 10番 | |
| 11番 Na |
12番 Mg |
13番 Al |
14番 | 15番 | 16番 硫黄 |
17番 塩素 |
18番 | |
| 19番 K |
20番 Ca |
|
||||||
| 銀 | 鉄 | |||||||
銅 |
||||||||
| 亜鉛 | ||||||||
| Ba | ||||||||
「また、覚え方は「水兵リーベ•••」という方法もありますが、そのような覚え方は価値を半減させます。1番『水素』は左の一番上、2番『ヘリウム』は右の端の一番上、3番から10番まではその下の位置する、11番から18番まではその下にある、という位置が重要です。原子周期表のおける位置、ポジションから即答できるようになれば本物です。例えば、軽くて周期表の中央部にある原子番号6番は•••? •••炭素、といえるようになれば、なぜ炭素が有機物と言われ、無限ともいえる化合物をつくることができるのか説明できるようになります」
(3)元素16種類それぞれの『単体』をつくる(15分)
「今日は、元素16種類の単体をすべて確認します。元素1つにつき1つの単体をつくります。では、原子番号1番から順にまとめていきましょう。原子番号1番『水素』からできる物質『水素』の化学式は? •••そうですね。H、ではなく、H2です。これは水素原子2個が結合して、水素という物質になっていることを示しています。H1でもH3でも物質『水素』としての性質を持っていません。水素爆発を起こす水素はH2です。次に覚えるものは原子番号6番『炭素』です。炭素の化学式は? •••そうですね。Cです。C2でもC3でもありません。これは炭素原子1個で炭素の性質を持っていることを示しています。次は原子番号7番『窒素』ですが、物質『窒素』の化学式は? •••そうですね。N、ではなく、N2です。これは •••(中略)••• 19番からはすべて金属になります。金属は原子1個で金属としての性質をもっているので原子記号を書くだけでよいです」
下表は、元素16種類について、それぞれの単体の作り方を2つに分けたものです。
① そのまま、でよいもの
② 右下に小さな2書くもの
| H2 水素 |
2番 | ||||||||
C |
N2 窒素 |
O2 酸素 |
|||||||
| Na ナトリウム |
Mg マグネシウム |
Al アルミニウム |
S 硫黄 |
Cl2 塩素 |
|||||
| K カリウム |
Ca カルシウム |
|
|||||||
| Ag 銀 |
Fe 鉄 |
||||||||
Cu |
|||||||||
| Zn 亜鉛 |
|||||||||
| Ba バリウム |
|||||||||
(4)金属の位置の確認(2.5分)
「ここで、金属について確認しておきましょう。金属は16個のうち10個です。かなりの割合ですね。元素全体からみても同じように割合は高く、元素92種類のうち金属は70種類もあります。さて、金属の作り方はさきほど紹介したように簡単です。原子記号を書くだけです。また、金属の位置についても確認しておきましょう。すべて周期表左側(下図)で、すべて『女の子』です。なぜ、左から2列目にたくさん並んでいるのかは、これからすぐに教えます」
| 1 | 2 | ||||||
| 3 | 4 | 5 | 6 |
7 | 8 | 9 | 10 |
| Na | Mg | Al | 14 | 15 | 16 | 17 | 18 |
| K | Ca | ||||||
| Ag | Fe | ||||||
Cu |
|||||||
| Zn | |||||||
| Ba | |||||||
(5)原子2個からできる単体=気体、と覚えればよい(2.5分)
「また、原子2個からできている物質についても確認しておきましょう。全部でいくつありますか? •••そうですね。水素、窒素、酸素、塩素の4つです。では、もう1つ質問です。これら4つの共通点はありますか? •••よくわかりましたね! すべて気体です。もちろん絶対零度に近づければ液体窒素や液体酸素になります。みなさんには1年生の時に、液体酸素を使って液体酸素をつくる実験を見せたと思います。しかし、常温、つまり普通の温度、25℃の場合はすべて気体の状態で存在する物質です。これらは分子とも言いますが、これについては2学期になってから教えます。予習したい人は教科書に書いてありますので、自分で調べておいてください」
| H2 水素 |
2 | ||||||
| 3 | 4 | 5 |
6 |
N2 窒素 |
O2 酸素 |
9 | 10 |
| 11 | 12 | 13 | 14 | 15 | 16 | Cl2 塩素 |
18 |
| 19 | 20 | ||||||
ここまでが授業前半です。5分ほど休息時間をとってもよいでしょう。本気の休息です。先生からの雑談もなし、です。何か発見した子どもは自主的にまとめ活動をすると思います。頭をフル回転させた子どもは机に伏せて休息すると思います。思い思いの方法でリフレッシュしてから、授業後半に入りましょう。以下は授業前半の2クラスの板書です。参考にしてください。ただし、それぞれのクラスの子どもに合わせて授業展開をしているので、違うまとめ方になっています。ご了承ください。

上:授業前半の板書(A組)
※周期表の縦列を意識させるため、水素•ナトリウム•カリウム•銀の順にまとめている
※O3(オゾン)が追加されている
※大気の組成(窒素78%、酸素21%、アルゴン1%)について記述されている
※←女子→ おかま ← 男子→ ニート、は授業後半開始に板書したもの

上:授業前半の板書(B組)
※前時のプリントと同じ手順(金属、希ガス、非金属のいくつか)(単体の分子)でまとめた
※O3(オゾン)が追加されている
※←女子→ おかま ← 男子→ ニート、は授業後半開始に板書したもの
(6)化合物の作り方(20分)
「前回も男女カップルのように化合物をつくりましたが、今回は名前から化学式をつくってもらいます。元素周期表を見てください。まず、男女の位置を確認しますね。左から3列は?••• その通り女子ですね。その次の列は?••• その通りおかまです。おかまとは、男女どちらとも仲良くできる、という意味です。次の3列は?••• その通り男子です。そして、残された右端1列は?••• その通り、誰とも仲良くならないという意味でニート、として紹介しました(上図参照)」
「化合物は『男女が化合してできて物質』ですが、その名前のつけ方は『男化女』です。(ここまでを上図のように板書してから)男子を確認すると、原子番号17番『塩素くん』だけです。この塩素くんを4人の女子と化合させてみます」
| 女 子 | おかま | 男 子 | ニート | ||||
| 水素 |
|
||||||
| ナトリウム | 塩素 | ||||||
| カリウム | |||||||
| 銀 | |||||||
「まず、男女とも両サイドのものを化合させてみましょう。周期表見てください。女子は4人いますが、男子は1人しかいませんね。したがって、組み合わせは何通りできますか? •••そうですね、4通りできます。この4通りすべてをまとめます」

上:男女の両サイドのものを化合させてできる化合物4種類
「原子番号1番の女子『水素さん』と化合した場合は、『塩素くん』化『水素さん』なので、塩素の素を取って『塩』化『水素』になります。(黒板に塩化水素と板書し、さらに、化に○をつける)塩化水素の化学式はとても簡単です。そのまま書くだけです。つまり、HCl(HClと板書する) これで完成です! 次の女子は『ナトリウムさん』もまったく同じよう化合させてみましょう。名前も化学式も同じように考えてください。ではここから順番に指名していきます。今日は11日なので11番の人から順に出席番号順に当てていきます。簡単なので近くの友だちに聞かないようにしてください。で、11番は誰ですか? はい、A君ですね。ではA君に問題です。塩素とナトリウムが化合した物質を何と言いますか? •••えっ、いきなりヒントですか! 簡単過ぎてヒントが難しいのですが、言いますよ。塩素と化合した水素は、塩化水素でしたね。塩素の素ととって『塩』にして、塩と化合した水素だから塩化水素でした。今の問題は、水素がナトリウムになっただけなので••• そうですね。塩化ナトリウムです。A君着席してください。次に、塩化ナトリウムの化学式を答えてもらいます。出席番号12番の人、お願いします! •••完璧です。NaClです。ただし、大文字と小文字の区別がしっかりできていない人はテストで×になりますので注意してください。次は、『カリウムさん』です。•••(後略)•••」
| 女 子 | おかま | 男 子 | ニート | ||||
|
|||||||
| 酸素 | |||||||
| マグネシウム | 硫黄 | ||||||
| カルシウム | |||||||
「次は、男女の中央のものをどうしを組み合わせます(上図)。原子番号20番までの場合、女子は2人、男子も2人になりますから、組み合わせとしては何通りできますか? •••ちょっと難しいかな? •••よくできました! 4通りです」
「名前も化学式もまったく同じようにつくります。つまり、酸素とマグネシウムが化合したものは? •••そうですね、酸化マグネシウムです。その化学式は? •••そうですね、MgOです。 酸素とカルシウムが化合したものは? •••そうですね、酸化カルシウムです。その化学式は? •••そうですね、CaOです。これら2つは酸素と化合したものなので、酸化物といいます(下図)」

上:2つの酸化物
「もう1人の男子『硫黄くん』と化合したものも同じように名前と化学式をつくることができます。ただし、酸素は素(そ)を取って『酸化』としましたが、硫黄は黄(おう)を取って『硫化』とします。硫化の読み方ですが、硫化(いか)ではありませんよ。硫化(りゅうか)です。硫化の硫(りゅう)は硫酸の硫(りゅう)で、硫酸にはS(硫黄)原子が含まれます。さて、『硫黄くん』との化合物を2つ作りましょう。まず、マグネシウムが化合したものは? •••そうですね、硫化マグネシウムです。その化学式は? •••そうですね、MgSです。 酸素とカルシウムが化合したものは? •••そうですね、硫化カルシウムです。その化学式は? •••そうですね、CaSです。これら2つは硫黄と化合したものなので、硫化物といいます(下図)」
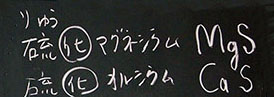
上:2つの硫化物
| 女 子 | おかま | 男 子 | ニート | ||||
|
|||||||
| 窒素 | |||||||
| アルミニウム | |||||||
「次は、男女の内側のものをどうしを組み合わせます(上図)。原子番号20番までの場合、女子『アルミニウムさん』、男子『窒素くん』しかいないので、組み合わせは? •••その通り、1通りしかありませんね」
「名前も化学式もまったく同じようにつくります。名前? •••そうです! よくわかりましたね。窒化(ちっか)アルミニウムです。聞き慣れないことばですが、正解です。窒素の素(そ)をとって窒素と化合したアルミニウム『窒化アルミニウム』になります。この物質は無色透明のとても固い物質です。さて、その化学式は? •••そうですね、AlNです(下図)」
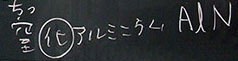
上:窒化アルミニウム

上:授業後半のここまでの板書
ここまでの(6-1)(6-2)(6-3)は男女比が1:1でカップルをつくっていましたが、次は男女の割合が違う場合を教えます。例えるなら、男好きな女子、女好きな男子がカップルをつくる場合です。
水の化学式はH2Oですが、H:O=2:1です。つまり、女子(Hさん)2人に対して、男子(Oくん)は1人です。
| 女 子 | おかま | 男 子 | ニート | ||||
| 1人 | 2人 | 3人 | 4人 |
3人 | 2人 | 1人 | 誰とも× 自分だけ |
| 水素 | |||||||
| 窒素 | 酸素 | ||||||
| ナトリウム | マグネシウム | アルミニウム | 硫黄 | 塩素 | |||
| カリウム | カルシウム | ||||||
| 女 子 | おかま | 男 子 | ニート | ||||
| 1人 | 2人 | 3人 | 4人 |
3人 | 2人 | 1人 | 誰とも× 自分だけ |
| 水素 | |||||||
| 窒素 | 酸素 | ||||||
| ナトリウム | マグネシウム | アルミニウム | 硫黄 | 塩素 | |||
| カリウム | カルシウム | ||||||
水素さんは1人、窒素くんは3人必要としています。したがって、水素:窒素=3:1、H3Nになります。ただし、アンモニアの化学式はH3Nです。例外的に男子•女子の順になります。この例外はアンモニアだけです。
化学式はすべて女子•男子の順に書く、と覚えてください。そして、男女比は小さな数字で表すこと、男女比は周期表を見ればわかることも覚えてください。
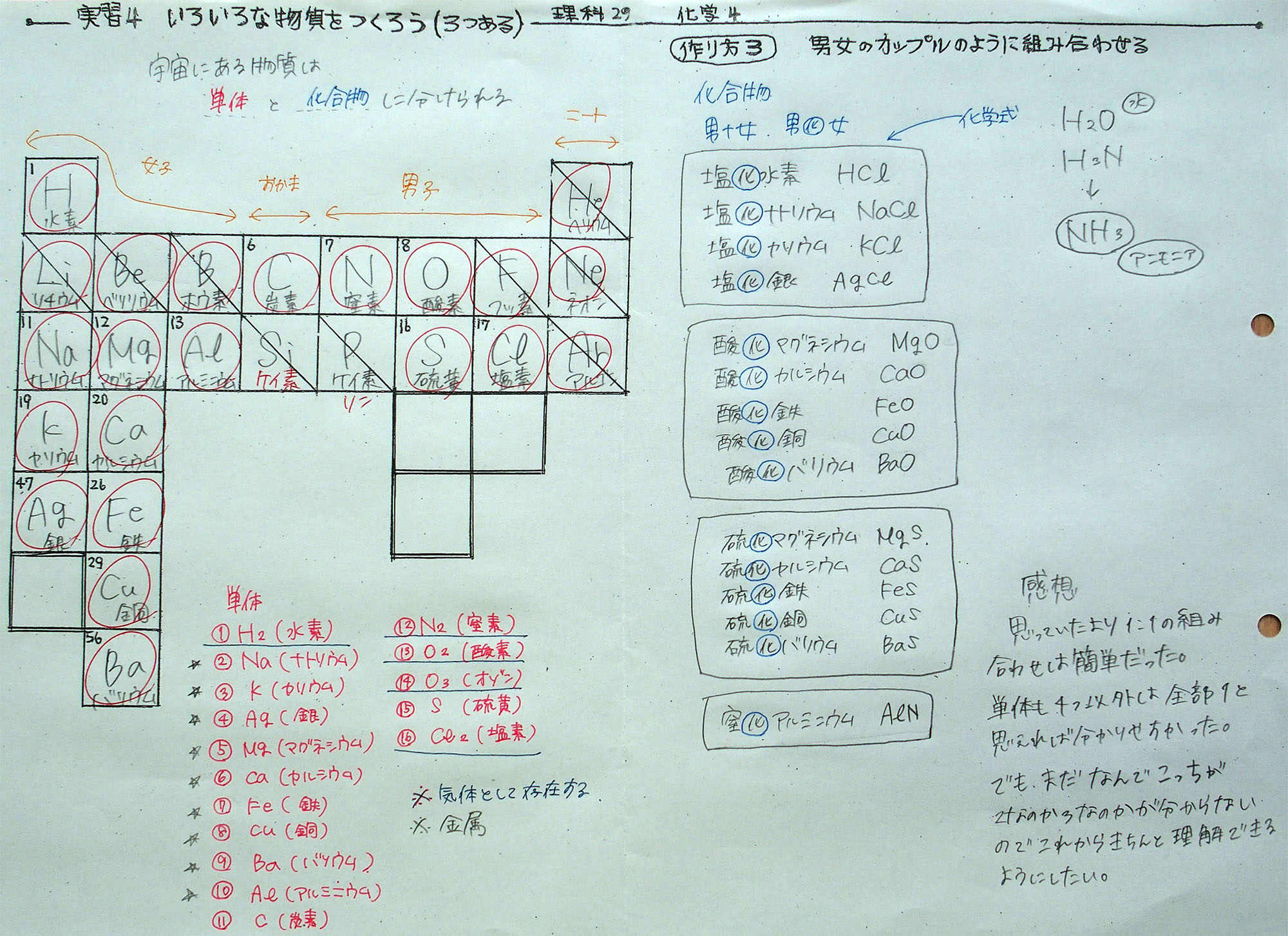
◎ 生徒の学習プリント

上:Aさんの学習プリント(クリックすると拡大)
※プリント右側に『酸化物』と『硫化物』がまとめてあります